Herz-Kreislauf-Erkrankungen sind die führenden Ursachen von Morbidität und Tod weltweit. Alters-assoziierte Veränderungen im arteriellen Eigenschaften, wie endotheliale Dysfunktion und strukturelle Veränderungen, werden als Initiale Ereignisse in der Entwicklung der Atherosklerose. Aufgrund der hohen Heterogenität des vaskulären Zellen aus unterschiedlichen Quellen, die unser Verständnis der menschlichen arterielle Alterung und die Entwicklung von Interventionen gegen humane arterielle Altern und damit verbundene Krankheiten sind behindert.
Kürzlich ist es Wissenschaftlern vom Institut für Zoologie der chinesischen Akademie der Wissenschaften und der Peking-Universität haben gemeinsam, und gründete die erste single-cell transkriptomischen atlas der Primaten arterielle Alterung.
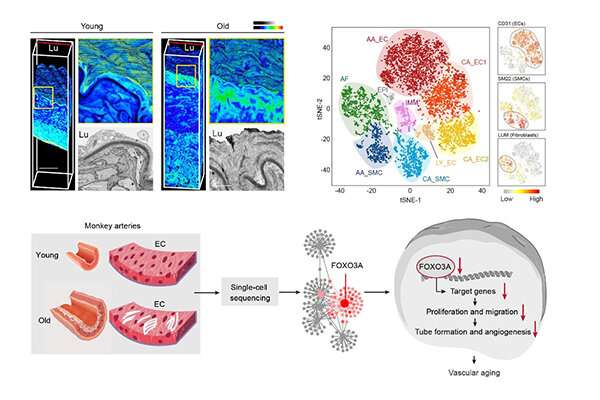
Mithilfe der einzelzell-Transkriptom-sequencing-Technologie, Sie zog eine umfassende aging-roadmap von cynomolgus Affen Arterien an der einzelligen Auflösung und identifiziert FOXO3A Verlust als ein wesentlicher Treiber für die arterielle Endothelzellen Altern.
Diese Studie mit dem Titel „single-cell-transkriptomischen Landschaft von Primaten arterielle Alterung“ wurde online veröffentlicht in Nature Communications , am 5. Mai 2020.
Die Aorta und die Koronararterien sind zwei der am häufigsten Verletzungs-anfällig Regionen im menschlichen Gefäßsystem mit dem Alter. Die Wissenschaftler analysierten die senile aortas, die ausgestellt Merkmale des vaskulären Alterns, einschließlich erhöhter Wanddicke, fibröse Kappe Bildung, Arterienverkalkung und elastische lamina Fragmentierung.
Dann schilderte die single-cell-transkriptomischen Landschaft der Arterien von Jungen und alten nicht-menschlichen Primaten und löste aorta oder koronar-Arterie-spezifische molekulare Signaturen für acht vaskulären Zelltypen.
Gen-Netzwerk-Analysen charakterisiert transkriptionelle Wahrzeichen, reguliert Kreislauf-Senilität und positioniert FOXO3A, eine Langlebigkeit-assoziierter Transkriptionsfaktor, der als master-regulator-Gens herunterreguliert in sechs Subtypen von monkey vaskulären Zellen während des Alterns.
Darüber hinaus gezielte Inaktivierung von FOXO3A in humanen arteriellen vaskulären Endothelzellen führte in der Störung der zellulären Homöostase und rekapituliert die wichtigsten phänotypischen defekte beobachtet, die im Alter von monkey Arterien.
Insgesamt richteten die Forscher eine high-resolution single-cell-transkriptomischen atlas von nicht-menschlichen Primaten arterielle Alterung ergeben, die dynamische Veränderungen in der Zelle, die Zusammensetzung und molekularen Eigenschaften während der arterielle Alterung in Primaten und verifiziert FOXO3A Verlust als ein wesentlicher Treiber für die arterielle Endothelzellen Altern.
Diese Arbeit stellt eine kritische Ressource für das Verständnis der Primaten arterielle Alterung und trägt wichtige Hinweise auf die zukünftige Behandlung von Alters-assoziierten vaskulären Erkrankungen.
Schließlich ist es bemerkenswert, dass das gleiche team kürzlich die weltweit erste FOXO3A-verbesserte menschliche vaskuläre Zellen mit gen-Editierung (Cell Stem Cell, 2019, cover-Artikel).
