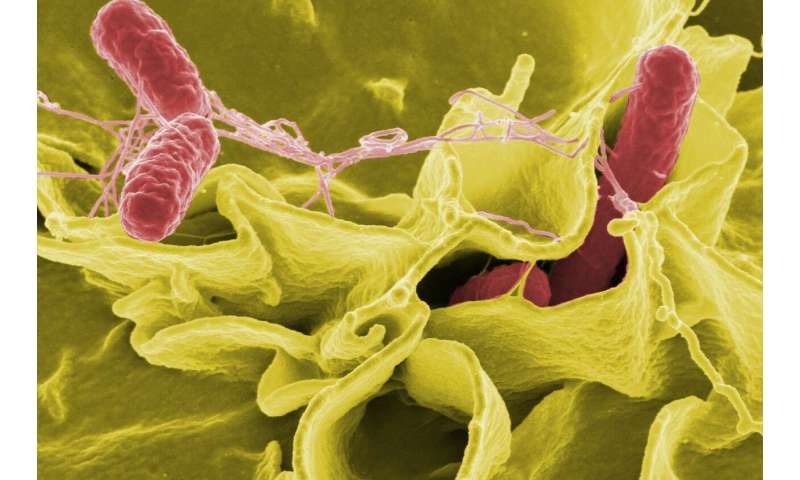
Wie die Infrastruktur eines Mehrfamilienhauses, einem faserigen protein, bekannt als curli-amyloid, das hergestellt wird durch Bakterien bietet den unterstützenden Rahmen für die Biofilm—Dicke extrazelluläre Substanzen aus Bakterien, die es ermöglichen, mehrere bakterielle Zellen zu montieren, zu überleben, und gedeihen, zusammen. Curli-amyloid, jedoch ist auch ein wichtiger Faktor bei Durchfall-Erkrankungen, hervorgerufen durch bakterielle Infektion, und Ihre schädlichen Auswirkungen erstrecken sich weit über den Magen-Darm-Trakt.
Insbesondere Infektionen mit Salmonella – Bakterien, die produzieren curli-amyloid, sind verwickelt in eine heimtückische, schmerzhafte entzündliche Erkrankung, bekannt als reaktive arthritis (ReA), das betrifft etwa fünf Prozent der Menschen, die infiziert wurden mit Bakterien, die zu Magen-Darm-Erkrankungen. Es gibt keine Behandlungen für ReA, und sehr wenig ist darüber bekannt, wie oder warum es sich entwickelt.
Jetzt in der neuen Arbeit, Forscher am Lewis Katz School of Medicine an der Temple University (LKSOM) zeigen, dass in Mäusen nach Infektion mit Salmonella enterica Typhimurium – eine häufige Ursache von lebensmittelbedingten Durchfallerkrankungen Krankheit—curli provoziert die Generierung von Autoantikörpern und Gelenkentzündungen. Die schädlichsten diese Effekte miteinander verknüpft wurden, um die systemische Exposition zu curli, enthüllt eine versteckte Schäden, die durch bakterielle Komponenten, die Flucht der Darm-Trakt.
Die Studie wurde online veröffentlicht 9. Juli in der Fachzeitschrift PLOS Pathogens.
„Wir fanden insbesondere, dass, wenn curli bleibt in den Darm, seine negativen inflammatorische Effekte begrenzt sind“, erklärt Cagla Tukel, Ph. D., Associate Professor in der Abteilung von Mikrobiologie und Immunologie an LKSOM und senior-Autor auf der neuen Studie. „Aber bei empfindlichen Personen, wenn curli entweicht aus dem Darm-Trakt und in den Kreislauf, eine Autoimmun-Reaktion entsteht.“
Die Forschung wurde durchgeführt in Zusammenarbeit mit Dr. Aaron P. Weiß und andere Wissenschaftler des Vaccine und Infektionskrankheiten Organisation-International Vaccine Centre, University of Saskatchewan, Kanada.
Dr. Tukel und Dr. White ‚ s laboratories entwickelten ein Mausmodell, in dem die Tiere wurden oral infiziert mit Wildtyp- S.-Typhimurium –, bedeutete, zu imitieren, Lebensmittel – oder Wasser-borne transmission in den Menschen. Das infektiöse inokulum Bestand aus S. Typhimurium – Zellen in der Lage, curli, obwohl keine curli wurde im inokulum selbst, wodurch die Forscher zu untersuchen, curli Produktion und Ihre Auswirkungen auf die Autoimmunität in vivo. Zum Vergleich, einige Mäuse infiziert waren, mit einem mutierten Stamm von S. Typhimurium unfähig curli-Produktion.
Innerhalb einer Woche nach der Infektion mit Wildtyp- S.-Typhimurium –, bakteriellen Clustern zeigten sich in den Blinddarm und Dickdarm von Mäusen, und wurden die Bakterien produzieren von curli. Eine orale Infektion weiter geführt, um die Generierung von Autoantikörpern gegen curli/DNA-komplexe, die entscheidend für die Biofilmbildung. Autoantikörper-Produktion zugeschrieben wurde, um die systemische Reichweite von curli.
Bewertung von Knie-Gelenke und serum von Mäusen, die mit Wildtyp- S.-Typhimurium bestätigt die systemische Anwesenheit von curli-induzierte Autoantikörper und Gelenkentzündungen. Darüber hinaus synovialen chronischen Entzündung, die die Flüssigkeit umliegenden Gelenke und Knochen-resorption (Knochen brechen), das sind die Markenzeichen von ReA, wurden beobachtet.
„Unsere Ergebnisse zeigen, dass curli ist eine wichtige Komponente von Salmonellen , die Laufwerke von Autoimmun-Reaktionen,“ Dr. Tukel sagte. „Bei Mäusen, die diese Reaktionen ausgelöst wurden, die innerhalb von sechs Wochen nach der Infektion, die belegen, dass die expression einer bakteriellen Komponente im Darm kann führen zu weiteren Autoimmun-Reaktionen.“
Ein protein, bekannt als HLAB27, die Herstellung, die verbunden ist mit einer bestimmten genetischen variation ist ein Risikofaktor für die Entwicklung von ReA. „Die Präsenz von pathogenen curli in der mikrobiota kann Niederschlag oder verschärfen Autoimmunität bei Patienten mit HLAB27,“ Dr. Tukel hingewiesen.
Dr. Tukel und Ihr team die Planung der nächsten, um zu bestimmen, ob die neuen Erkenntnisse auf den Menschen übertragen, und ob curli-Proteine von anderen pathogenen Bakterien, wie E. coli, sind in der Lage erzeugen ähnliche autoimmune Reaktionen. Ihre Gruppe wird auch untersucht, ob curli eine Rolle spielt, übertreibt anderen Autoimmunerkrankungen, wie dem systemischen lupus erythamatosus (SLE), in denen genetische Risikofaktoren beteiligt sind.
