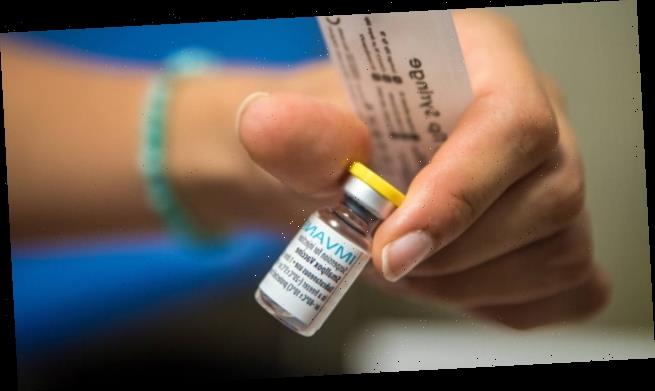
Auf den ersten Blick wirkt Impfen nicht wie ein besonders komplizierter Handgriff. Doch die Empfehlung zur Aspiration bei der intramuskulären COVID-19-Impfung hat Anfang des Jahres gezeigt, dass es manches zu beachten gilt. Interessant ist deshalb auch, dass Imvanex, der subkutan zu applizierende Impfstoff gegen Affenpocken, laut EMA jetzt intradermal statt subkutan verabreicht werden kann – allerdings nur von erfahrenem Fachpersonal.
Die US-amerikanische Arzneimittelbehörde FDA empfiehlt sie schon seit dem 9. August, die europäische (EMA) seit vergangenem Freitag: die intradermale Anwendung des Impfstoffs gegen Affenpocken, der in den USA Jynneos und in Europa Imvanex heißt. Zugelassen ist der Impfstoff zwar auch in Europa bereits seit Ende Juli, die Empfehlung für die Impfung für Risikogruppen steht bereits seit Juni –, allerdings für die subkutane Applikation.
Intradermal bedeutet, dass der Impfstoff auch direkt unter der obersten Hautschicht appliziert werden kann. So wird laut EMA weniger Impfstoff benötigt als bei der subkutanen Applikation. „Angesichts des derzeit begrenzten Angebots an Impfstoffen bedeutet dies, dass mehr Menschen geimpft werden können“, erklärt die EMA.
Mehr zum Thema
Wenn die Impfung nicht reicht
Tecovirimat – ein Arzneimittel gegen Affenpocken

Risikogruppen aufklären
Wer sich gegen Affenpocken impfen lassen sollte
EU-Kommission
Imvanex erhält EU-Zulassung für Affenpocken
In einer klinischen Studie mit rund 500 Erwachsenen habe sich gezeigt, dass zwei subkutane Dosen zu je 0,5 ml im Abstand von vier Wochen ähnliche Antikörper-Spiegel erzeugten wie ein Fünftel der Dosis (0,1 ml) intradermal appliziert. Allerdings bringt dieser Applikationsweg mehr lokale Nebenwirkungen mit sich, wie länger anhaltende Rötung und Verdickung oder Verfärbung der Haut. Außerdem ist nicht klar, wie viele 0,1-ml-Dosen tatsächlich aus den 0,5 ml gewonnen werden können. Um die Anzahl zu optimieren, sollen Spritzen mit geringem Totvolumen genutzt werden. Und auch nach Beachtung dieser Hinweise ist die intradermale Applikation noch kein „Selbstläufer“. Die EMA empfiehlt, dass nur medizinisches Fachpersonal mit Erfahrung zur intradermalen Injektion die Impfungen so verabreichen soll.
Weitere Details erläutert die EMA in einem gesonderten Dokument. Demnach handelt es sich bei Imvanex um einen nicht replizierenden abgeschwächten Lebendimpfstoff der dritten Generation, der auf dem „modifizierten Vaccinia Ankara – Bavarian Nordic Vektor“ (MVA-BN) basiert. Die intradermale Verabreichung zur Antigeneinsparung sei für mehrere Impfstoffe zugelassen – insbesondere für BCG (Tuberkuloseimpfstoff), Influenza- und Tollwutimpfstoffe.
Das Impfschema
„Die Grundimmunisierung sollte mit zwei Impfstoffdosen in einem Abstand von ≥ 28 Tagen erfolgen (subkutane Applikation). Bei Personen, die in der Vergangenheit bereits gegen Pocken geimpft wurden, reicht eine einmalige Impfstoffgabe aus.“
(Quelle: STIKO, 9. Juni 2022)
Dass die intradermale Applikation zu signifikant mehr lokalen unerwünschten Reaktionen führt – wie Erytheme und Verhärtungen – sei in einer Studie von 2010 zu einem anderen MVA-Impfstoff gezeigt worden: Dort berichteten rund 30 Prozent mehr Proband:innen mit intradermaler Applikation (als bei subkutaner Applikation) nach der ersten Dosis über lokale Reaktionen und etwa 20 Prozent nach der zweiten. Die Reaktionen sollen nach der zweiten Dosis stärker gewesen sein.
Alle Impfungen zusammengenommen, betrug der Anteil der Proband:innen mit ausgeprägten Erythemen oder Verhärtungen an der Injektionsstelle (> 30 mm) 58,1 Prozent in der subkutanen Gruppe und 94,8 Prozent in der intradermalen Gruppe. Zudem kam es bei 25 Prozent der subkutanen Gruppe zu lokalen Reaktionen, die mindestens 30 Tage andauerten, unerwarteten Knötchen und Hautverfärbungen – mit 67 Prozent waren es in der intradermalen Gruppe mehr. Was systemische Reaktionen betrifft, soll es zwischen beiden Applikationswegen jedoch keine Unterschiede gegeben haben.
Noch viele Unbekannte
Die EMA betont insgesamt, dass das genaue Ausmaß und die genaue Dauer des Schutzes durch die Impfung nicht bekannt sind. Wie die EMA im Juli erklärte, stützt sich die Zulassung auf Daten aus mehreren Tierstudien. Diese sollen einen Schutz gegen das Affenpockenvirus bei mit Imvanex geimpften (nicht menschlichen) Primaten gezeigt haben. Um die Wirksamkeit zu bestätigen, werde der Zulassungsinhaber Bavarian Nordic zudem Daten in einer Beobachtungsstudie sammeln, die während des aktuellen Affenpockenausbruchs in Europa durchgeführt werde, hieß es.
Es sei nun wichtig zu beachten, dass die intradermale Applikation von einem Zwei-Dosis-Regime ausgeht. Deshalb müsse bedacht werden, dass die starken lokalen Reaktionen bei manchen Patient:innen dazu führen könnten, dass sie sich kein zweites Mal impfen lassen – was einen verminderten Schutz bedeuten könnte. Es ist auch nicht klar, wie die reduzierte intradermale Dosis für besondere Patientengruppen wie Immunsupprimierte einzuschätzen ist. Zudem gibt es keine Stabilitätsdaten zum geöffneten Impfstoff. Weitere begleitende Untersuchungen werden also benötigt. Damit kommt die EMA zu dem Schluss:
Quelle: Den ganzen Artikel lesen